Bezpieczeństwo i tolerancja RAVICTI®1,2
Stosowanie RAVICTI® (fenylomaślan glicerolu) jest wszechstronnie udokumentowane w leczeniu zaburzeń cyklu mocznikowego.
Ocenę działań niepożądanych związanych z produktem RAVICTI przeprowadzono w programie badawczym opartym na ekspozycji u 114 pacjentów z UCD (65 dorosłych i 49 dzieci w wieku od 2 miesięcy do 17 lat) z niedoborami CPS, OTC, ASS, ASL, ARG lub z zespołem HHH. Dodatkowe działania niepożądane oceniano w badaniu klinicznym obejmującym 16 pacjentów z UCD w wieku poniżej 2 miesięcy.
Na początku leczenia mogą wystąpić bóle jamy brzusznej, nudności, biegunka i/lub ból głowy. Reakcje te zwykle ustępują w ciągu kilku dni, nawet jeśli leczenie jest kontynuowane.
Najczęstsze działania niepożądane zgłaszane w badaniach klinicznych (co najmniej 10% pacjentów):
- Pacjenci dorośli: biegunka, wzdęcia, ból głowy, nudności, wymioty, zmniejszony apetyt, zawroty głowy i zmęczenie
- Pacjenci pediatryczni w wieku od 2 do 17 lat: ból w nadbrzuszu, wysypka, nudności, wymioty, biegunka, zmniejszony apetyt i ból głowy
- Pacjenci pediatryczni w wieku od 2 miesięcy do mniej niż 2 lat: neutropenia, wymioty, zaparcia, biegunka, gorączka, osłabienie zdolności połykania, kaszel, przekrwienie błony śluzowej nosa, wyciek z nosa, wysypka i grudki
- Pacjenci pediatryczni w wieku poniżej 2 miesięcy: wymioty, wysypka, refluks żołądkowo-przełykowy, zwiększenie aktywności enzymów wątrobowych, zaburzenia odżywiania (zmniejszenie apetytu, osłabienie zdolności połykania), niedokrwistość, kaszel, odwodnienie, kwasica metaboliczna, trombocytoza, trombocytopenia, neutropenia, limfocytoza, biegunka, wzdęcia, zaparcia, gorączka, letarg i drażliwość/pobudzenie
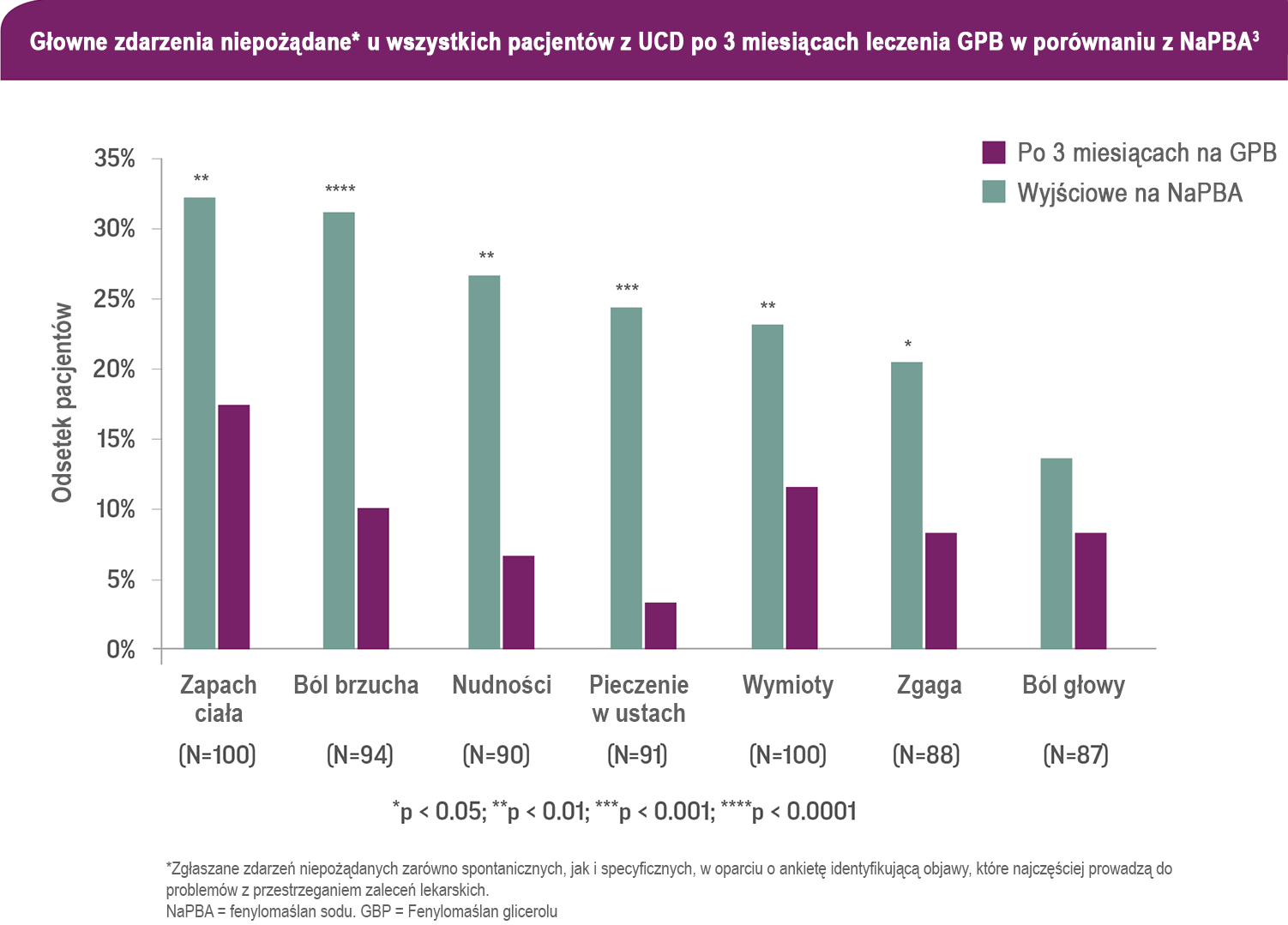
Zdarzenia niepożądane związane z leczeniem – RAVICTI w porównaniu do NaPBA
Stu pacjentów lub ich opiekunów odpowiedziało na niezatwierdzony kwestionariusz specyficzny dla UCD, zawierający wcześniej ustaloną listę typowych objawów związanych ze stosowaniem zmiataczy azotu. Wartości wyjściowe (gdy pacjenci otrzymywali fenylomaślan sodu [NaPBA]) porównano z wartościami po trzech miesiącach leczenia fenylomaślanem glicerolu (ang. glycerol phenylbutyrate, GPB).3
Specjalne ostrzeżenia i środki ostrożności dotyczące stosowania
Nawet podczas leczenia fenylomaślanem glicerolu u części pacjentów może wystąpić ostra hiperamonemia, w tym encefalopatia hiperamonemiczna.
- Nadwrażliwość na substancję czynną
- Leczenie ostrej hiperamonemii
Zewnątrzwydzielnicze enzymy trzustkowe powodują hydrolizę glicerolu fenylomaślanu w jelicie cienkim, oddzielając aktywny fragment cząsteczki, fenylomaślan, od glicerolu. Proces ten umożliwia wchłanianie fenylomaślanu do krwiobiegu. Mała ilość lub brak enzymów trzustkowych, albo choroba jelit skutkująca zaburzeniem wchłaniania tłuszczów może spowodować obniżenie lub brak trawienia glicerolu fenylomaślanu lub też obniżenie lub brak wchłaniania fenylomaślanu i gorszą kontrolę stężenia amoniaku w osoczu. Stężenie amoniaku należy ściśle monitorować u pacjentów z niewydolnością trzustki lub zaburzeniami wchłaniania jelitowego.
- U pacjentów z nowotworem, którzy otrzymali kwas fenylooctowy dożylnie, zgłaszano odwracalne objawy kliniczne wskazujące na neurotoksyczność (np. nudności, wymioty, senność) związaną ze stężeniem fenylooctanu w zakresie 499–1285 mikrogramów/ml. Choć podobnych obserwacji nie odnotowano w badaniach klinicznych z udziałem pacjentów z zaburzeniami cyklu mocznikowego, należy podejrzewać wysokie stężenie kwasu fenylooctowego u pacjentów (w szczególności u dzieci w wieku poniżej 2 miesięcy) z niewyjaśnioną sennością, splątaniem, nudnościami i letargiem, u których stwierdzono prawidłowe lub niskie stężenie amoniaku.
- Jeśli objawy takie jak wymioty, nudności, bóle głowy, senność, splątanie lub ospałość występują przy braku wysokiego stężenia amoniaku lub innych chorób współistniejących, należy zmierzyć stężenie kwasu fenylooctowego w osoczu oraz stosunek stężenia kwasu fenylooctowego do fenyloacetyloglutaminy w osoczu i jeżeli stężenie kwasu fenylooctowego przekracza 500 mikrogramów/l oraz stosunek stężenia kwasu fenylooctowego do fenyloacetyloglutaminy w osoczu przekracza 2,5, należy rozważyć zmniejszenie dawki glicerolu fenylomaślanu lub zwiększenie częstości podawania dawek w ciągu doby.
Dawkę dobową należy indywidualnie dostosować z uwzględnieniem ewentualnej szacunkowej zdolności do syntezy mocznika, profilu aminokwasowego, tolerancji białka i dziennego spożycia białka w diecie, niezbędnego do prawidłowego wzrostu i rozwoju. Podawanie preparatów uzupełniających dietę w aminokwasy może być niezbędne do utrzymania prawidłowego stężenia niezbędnych aminokwasów i aminokwasów o rozgałęzionych łańcuchach. Dalsze dostosowywanie dawki może być oparte na monitorowaniu stężenia amoniaku w osoczu, glutaminy, fenyloacetyloglutaminy w moczu i (lub) kwasu fenylooctowego i fenyloacetyloglutaminy w osoczu, oraz stosunku stężenia kwasu fenylooctowego do fenyloacetyloglutaminy w osoczu (patrz punkt 4.2 w ChPL).
Kortykosteroidy
Stosowanie kortykosteroidów może powodować rozpad białek ustrojowych i zwiększać stężenie amoniaku w osoczu. W przypadku jednoczesnego stosowania kortykosteroidów i fenylomaślanu glicerolu należy ściśle monitorować stężenie amoniaku.
Kwas walproinowy i haloperydol
Podczas stosowania haloperydolu i kwasu walproinowego może dojść do hiperamonemii. Podczas stosowania haloperydolu lub kwasu walproinowego u pacjentów z zaburzeniami cyklu mocznikowego należy ściśle monitorować stężenie amoniaku
Probenecyd
Probenecyd może hamować wydalanie metabolitów glicerolu fenylomaślanu przez nerki, w tym fenyloacetyloglutaminy.
Kobiety w wieku rozrodczym muszą stosować skuteczne środki antykoncepcyjne (patrz punkt 4.6 ChPL).
Produktu RAVICTI nie należy stosować w okresie ciąży oraz u kobiet w wieku rozrodczym, które nie stosują antykoncepcji, chyba że stan kliniczny kobiety wymaga leczenia fenylomaślanem glicerolu, patrz punkt 4.6 ChPL.
Zgłaszanie zdarzeń dotyczących bezpieczeństwa
Osoby należące do fachowego personelu medycznego powinny zgłaszać wszelkie podejrzewane działania niepożądane. Zdarzenia niepożądane powinny zostać zgłoszone. Zdarzenia niepożądane należy zgłaszać spółce Immedica za pośrednictwem poczty elektronicznej na adres: safety@immedica.com
W razie konieczności zgłoszenia reklamacji produktu, należy to robić zgodnie z wymogami krajowymi a w pierwszej kolejności w lokalnej aptece. Można również skontaktować się z Immedica Quality pod adresem: complaints@immedica.com
Źródła:
1. RAVICTI European Assessment Report.
2. Charakterystyka Produktu Leczniczego RAVICTI.
3. Nagamani SC et al. Mol Genet Metab. 2015;116:29–34.

