Zaburzenia cyklu mocznikowego (UCD) – podstawowa przyczyna i obraz kliniczny1
- Zaburzenia cyklu mocznikowego to bardzo rzadkie, poważne i zagrażające życiu zaburzenia obejmujące grupę dziedzicznych niedoborów jednego z enzymów lub transporterów biorących udział w cyklu mocznikowym, który przekształca amoniak w mocznik
- Brak lub poważna dysfunkcja enzymów albo transporterów powoduje wystąpienie toksycznego poziomu amoniaku we krwi i mózgu u dotkniętych chorobą pacjentów
- Istnieje sześć różnych typów UCD, po jednym dla każdego enzymu w cyklu mocznikowym:
- NAGS – niedobór syntazy N-acetyloglutaminianowej*
- CPS 1 – niedobór syntazy karbamoilofosforanowej I
- OTC – niedobór karbamoilotransferazy ornitynowej
- ASS – niedobór syntetazy argininobursztynianowej, zwany też cytrulinemią typu I
- ASL – niedobór liazy argininobursztynianowej, zwany również kwasicą argininobursztynianową
- ARG – niedobór arginazy
- Istnieją również dwa niedobory transportera enzymów, które są również uważane za UCD:
- HHH – niedobór translokazy ornitynowej, zwany także zespołem Hiperornitynemii-Hiperamonemii-Homocytrulinurii
- CTLN2 – niedobór cytrynu lub cytrulinemia typu II*
- Chociaż genetycznie odmienne, UCD mają wspólne ważne cechy i dlatego są zazwyczaj uważane za grupę
- UCD dotyka około 1 na 35 000 osób, a objawy różnią się w zależności od osoby i mogą występować w różnym wieku
* Należy pamiętać, że RAVICTI nie jest dopuszczony do leczenia chorób powstałych w związku z niedoborami NAGS i CTLN2
Cykl mocznikowy
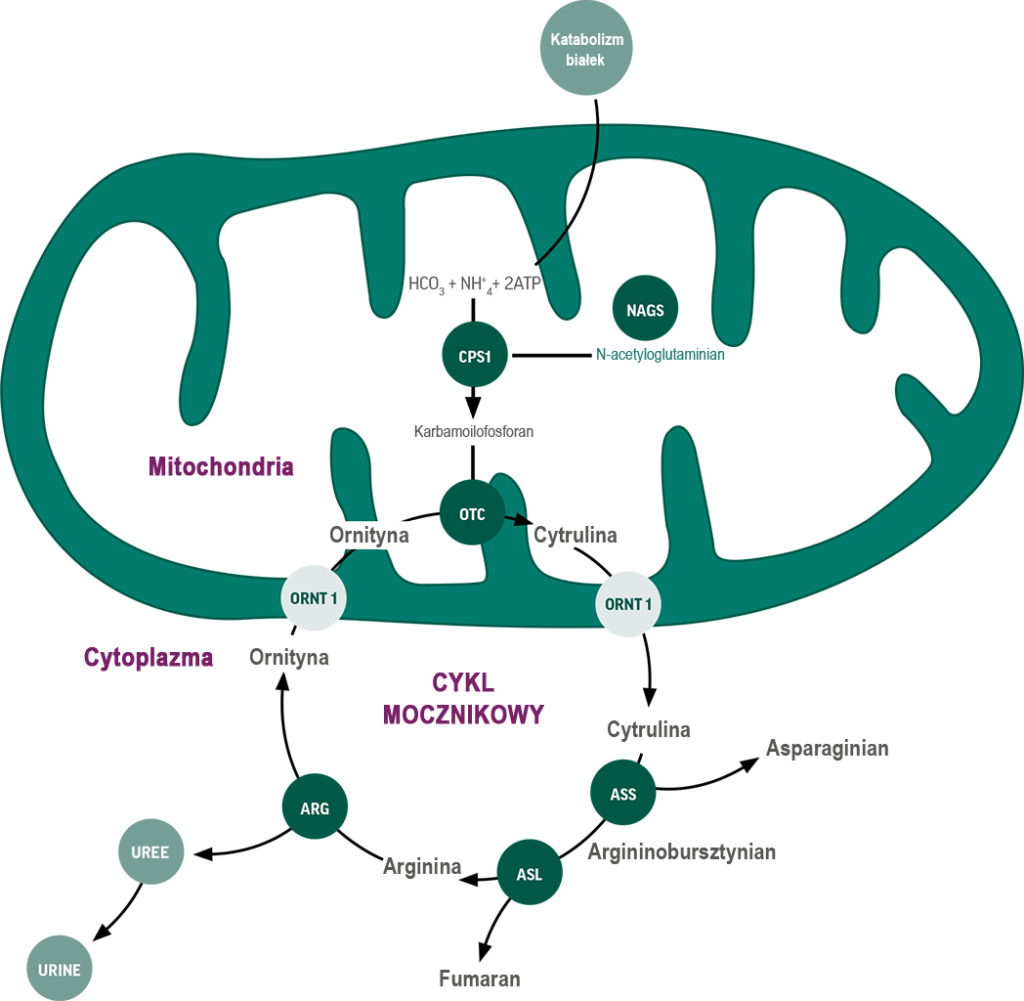
6 enzymów
NAGS = syntaza N-acetyloglutaminianowa
CPS1 = syntaza karbamoilofosforanowa I
OTC = karbamoilotransferaza ornitynowa
ASS = syntetaza argininobursztynianowa
ASL = liaza argininobursztynianowa
ARG = arginaza
1 nośnik
ORNT1 = translokaza ornitynowa
Korelacja między stężeniami amoniaku a objawami klinicznymi
- Podwyższone stężenia amoniaku prowadzą do rozwoju charakterystycznych objawów, a nieleczone prowadzą ostatecznie do przełomu hiperamonemicznego.1,2
- Wczesne objawy u dotkniętych chorobą noworodków są niespecyficzne, ale mogą szybko doprowadzić do śpiączki i śmierci.3,4
- Skutki przewlekłej hiperamonemii mogą wydawać się subtelne i niespecyficzne, co może ukrywać postępujące ryzyko UCD.3,5,6
- Bez względu na wiek zachorowania, wszyscy pacjenci chorzy na zaburzenie cyklu mocznikowego są narażeni na poważne konsekwencje neurologiczne i przedwczesną śmierć.4,6
Amoniak
(µmol/l)
>250
a
Powyżej GGN
GGN
Potencjalne objawy
Yes, we will adjust it on the website
- Śpiączka
- Obrzęk mózgu
- Objawy psychiatryczne (omamy, obłęd, stan pobudzenia maniakalnego)
- Senność
- Letarg
- Wymioty
- Postępujący słaby apetyt
Subtelne objawy
Norma
GGN = górna granica normy. GGN jest ustalana indywidualnie dla każdego laboratorium szpitalnego.
W badaniach klinicznych Ravicti, GGN zdefiniowano jako 35 μmol/l.7
Ammonia (NH3)
(umol/l)
>250
61-200
36-60
≤35
(ug/dl)
>450
110-360
65-108
≤63
>450
Potential symptom(s)
Hyperammonaemic coma
Coma
Cerebral oedema
Vomiting
Disorientation
Somnolence
Lethargy
Irritability
Anorexia
Subclinical hyperammonaemia
Normal
Konsekwencje wzrostu steżenia amoniaku są nieprzewidywalne
- Różnice dobowe stężenia amoniaku mogą być 10-krotne.8
- Hiperamonemia może być wywołana normalnymi zdarzeniami życiowymi, takimi jak choroba, spożywanie alkoholu, ciąża, zabieg chirurgiczny i wypadki.9-10
Leczenie zaburzenia cyklu mocznikowego
Celem przewlekłego leczenia zaburzenia cyklu mocznikowego jest utrzymanie stężenia amoniaku we krwi na bezpiecznym, niskim poziomie, utrzymanie stabilnej kontroli metabolicznej, eliminacja przewlekłych powikłań oraz osiągnięcie normalnego rozwoju i wzrostu.11
Długotrwałe leczenie polega na zmniejszeniu zawartości białka w diecie wraz z podawaniem farmaceutyków (np. zmiataczy azotu) oraz suplementacją niezbędnych aminokwasów, witamin i pierwiastków śladowych. Dodatkowe możliwości leczenia niektórych pacjentów to dializa lub przeszczep wątroby.11
RAVICTI® (fenylomaślan glicerolu) to zmiatacz azotu stosowany u pacjentów w każdym wieku chorych na UCD, ułatwiający podawanie i przestrzeganie reżimu leczenia.7,12
Źródła:
1. Summar M, Tuchman M. J Pediatr. 2001;138(1):6–10.
2. Häberle J et al. J Inherit Metab Dis. 2019;1–39.
3. Ah Mew N et al. W: Pagon RA, et al, eds. GeneReviews. Seattle, WA: University of Washington, Seattle; 2015. http://www.ncbi.nlm.nih.gov/books/NBK1217/. Ostatni dostęp 21.10.2020.
4. Cohn RM et al. Clin Pediatr (Phila). 2004;43:683-689.
5. Gropman AL et al. Metab Brain Dis. 2013;28:269–275.
6. Häberle J et al. Orphanet J Rare Dis. 2012;7:32.
7. Diaz GA et al. Hepatology. 2013;57(6):2171–2179.
8. Mokhtarani M et al. Mol Genet Metab. 2012;107:308–314.
9. Summar ML et al. Acta Paediatr. 2008;97:1420–1425.
10. McGuire PJ et al. J Pediatr. 2013;163:1705–1710.
11. Häberle Jz, McCandless S. Orphan drugs in development for UCDs, Orphan Drugs Research and Reviews 2014.
12. Charakterystyka Produktu Leczniczego RAVICTI.

